Упрощенная HTML-версия
Желто-зеленую флуоресценцию наблюдают в ультрафиолетовом свете при
длине волны 254 им у водного 0,1%-ного раствора рибофлавина-мононуклеотида.
Она исчезает при добавлении 1%-ного раствора гмдроксида натрия или
разведенной хлороводородной кислоты.
Рибофлавина-мононуклеотид
в
отличие
от
рибофлавина
дает
положительную реакцию на ион натрия и на фосфаты, которые образуются после
кипячения в течение 5 мин раствора в концентрированной азотной кислоте. Кроме
того, определяют (без разрушения) содержание примеси фосфорной кислоты (не
более 0,7%) спектрофотометрическим методом, используя в качестве реактива
молибдат аммония при длине волны 740 им.
Как
азотсодержащее
органическое
основание
,
рибофлавин
дает
положительную реакцию с реактивом Драгендорфа и другими осадительными
реактивами.
Реакции комплексообразования.
С солями металлов (серебра, кобальта, меди,
ртути и др.) рибофлавин образует нерастворимые окрашенные комплексные
соединения. Например, с раствором нитрата серебра — ораижево красного,
переходящего в красный, а с солями ртути ( — оранжевого цвета. Эти реакции
используют для фотоколориметрического определения рибофлавина в
лекарственных формах.
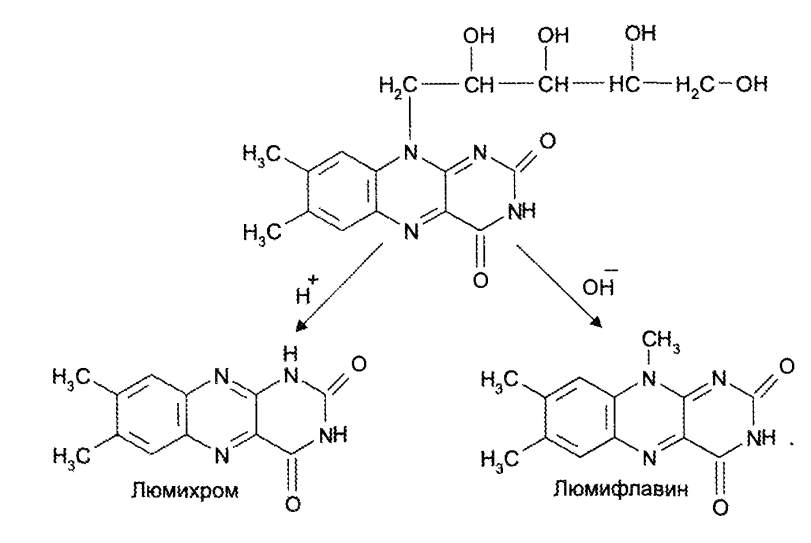
Определение чистоты
. В рибофлавине и рибофлавина-мононуклеотиде
устанавливают допустимое содержание принеси люмифлавина путем извлечения
его хлороформом. Затем либо измеряют его оптическую плотность относительно
хлороформа при длине волны 440 им (рибофлавин), либо сравнивают окраску
хлороформного извлечения от носительно раствора дихромата калия определенной
концентрации (рибофлавина-мононуклеотид).
Способы количественного определения
титриметрическими методами
основаны
на
использовании
ки
слотно-основных
и
окислительно-
восстановительных свойств.

