Упрощенная HTML-версия
оптических плотностей при 373 нм и 267 им должно быть в пределах от 0,31 до
0,33, а при 444 нм и 267 им — от 0,36 до 0,39.
Допустимое
содержание
поглощающих
примесей
в
рибофлавина
мононуклеотиде устанавливают, измерив оптическую плотность его раствора при
длинах волн 373 им, 266 им и 445 им. Отношение этих величин при 373 и 445 нм
должно быть от 0,83 до 0,86, а при 266 и 445 им — от 2,5 до 2,75.
Химические методы анализа.
Для испытаний производных изоаллоксазина используют химические реакции,
основанные на окислительно-восстановительных свойствах сопряженных двойных
связей,
окислении
и
этерификации
рибитильной
части
молекулы,
комплексообразовании, гидролизе, наличии в молекуле третичного атома азота,
иона натрия и связанной фосфорной кислоты.
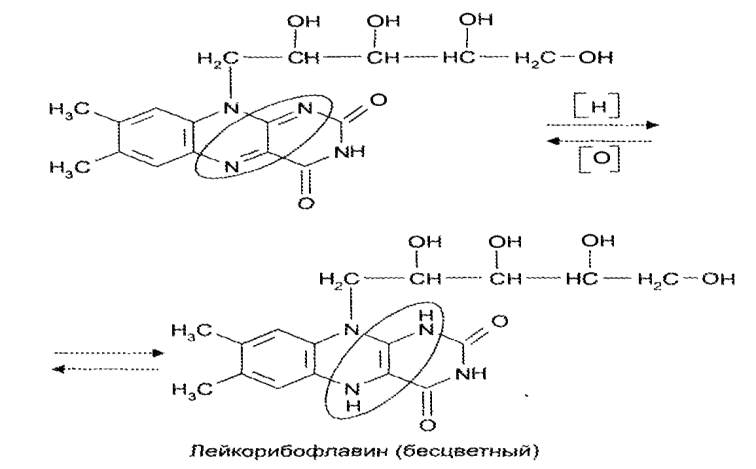
Окислительно-восстановительные свойства
рибофлавина и его производных
связаны с наличием сопряженной изоаллоксазиновой системы. Восстановление
рибофлавина приводит к образованию бесцветного лейкорибофлавина, который
может окисляться до характерно окрашенного рибофлавина:
В качестве реактива используют также концентрированную серную кислоту, от
которой при смачивании крупинка рибофлавина приобретает вишнево-красное
окрашивание.
Раствор нингидрина при кипячении в щелочной среде образует в присутствии
рибофлавина зеленую окраску.
Флюоресценция.
Разбавленный раствор рибофлавина в воде имеет яркую зеленую
флюоресценцию при подсвечивании в УФ-свете, исчезающую при добавлении как
раствора кислоты, так и раствора щелочи.
Добавление гидросульфита натрия приводит к исчезновению и флюоресценции,
и окрашивания.
При действии кислоты и УФ-света образуется люмихром (производное
изоаллоксазина), а при действии щелочи — люмифлавин (производное
изоаллоксазина):

