Упрощенная HTML-версия
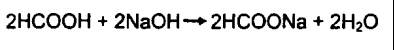
Для
количественного
определения
применяют
алкалиметрическое
определение рибофлавина после его реакции с нитратом серебра,
а также
цериметрию с иодометрическим окончанием и метод Кьельдаля (содержание азота
14,5— 15,2%). Предполагают, что под действием нитрата серебра происходит
замещение водорода иминогруппы ионом серебра с выделением эквивалентного
количества азотной кислоты, которую отгитровывают щелочью (индикатор
бромтимоловый синий).
При цериметрическом определении
0,02 М раствором сульфата церия (
окисляют рибофлавин при кипячении (в течение 1 минуты). Затем после
охлаждения добавляют иодид калия и титруют выделившийся иод.
Селективными,
позволяющими количественно определять содержание
рибофлавина, являются методики, базирующиеся на реакциях по рибитильному
радикалу, влияющему на витаминную активность.
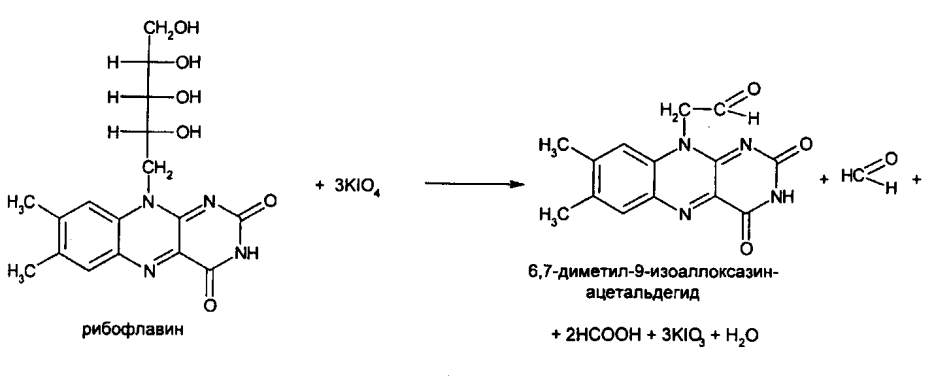
Одна из таких методик основана на окислении рибофлавина 0,02 М раствором
периодата калия в нейтральной среде при комнатной температуре с образованием
муравьиной кислоты. Ее количество эквивалентно
взятому на определение рибофлавину:
Выделившуюся муравьиную кислоту отгитровывают алкалиметрическим
методом:
Второй способ определения рибофлавина по рибитильной части молекулы
основан на этерификации
концентрированной серной кислотой. При этом за счет
гидроксильных
групп
происходит
образование
моно-,
ди-,
три-,
тетрасульфокислотных эфиров. Затем потенциометрическим титрованием
раствором гидроксида калия устанавливают избыток серной кислоты. Реакция
протекает стехиометрически в соотношении 1:3.
Хранение
. Рибофлавин необходимо хранить в хорошо укупоренных банках
оранжевого стекла, учитывая его свойство легко окисляться и разлагаться под
действием света с образованием биологически неактивных люмихрома и
люмифлавина. Рибофлавина-мононуклеотид более устойчив, поэтому его хранят в
сухом, защищенном от света месте.

