Упрощенная HTML-версия
применяют для выделения и разделения ионов сложной смеси.
Селективные -
аналитические сигналы одинаковы для ограниченного
количества ионов. Реагент - селективный. Пример: при действии реагента
NH
4
SCN на смесь катионов только два катиона образуют окрашенные
комплексные соединения: кроваво-красное [Fe(SCN)
6
]
3-
и синее [Co(SCN)
4
]
2-
Специфические -
аналитический сигнал характерен только для одного иона.
Реагент - специфический. Таких реакций крайне мало.
2. По типу аналитического сигнала:
Цветные
Осадительные
Газовыделительные
Микрокристаллические
3. По функции:
Реакции обнаружения (идентификации)
Реакции разделения (отделения)
для удаления мешающих ионов путем
осаждения, экстракции или возгонки.
3.2. Техника выполнения аналитических реакций.
При анализе неорганических катионов чаще всего применяют реакции, происходящие в
водных растворах между определяемыми ионами и реагентом. При этом по технике
выполнения различают следующие реакции:
Реакции в пробирке.
Исследуемый раствор (2-3 капли) вносят в пробирку
капиллярной пипеткой так, чтобы кончик пипетки не коснулся стенок пробирки.
Соблюдая условия проведения реакции, прибавляют 2-3 капли реагента. Наблюдают
внешний эффект реакции.
Капельные реакции.
Каплю раствора реагента наносят на полоску фильтровальной
бумаги капилляром, для чего концом капилляра прикасаются к бумаге. Пятно должно
быть круглым с диаметром 2-3 мм. В центр полученного пятна аналогично наносят
каплю исследуемого раствора. Наблюдают внешний эффект реакции. При выполнении
реакций на фильтровальной бумаге используются адсорбционные свойства бумаги.
Капля жидкости, нанесенная на бумагу, быстро рассасывается по капиллярам, а
окрашенное соединение адсорбируется на небольшой площади листа. При наличии в
растворе нескольких веществ скорость движения их может быть различной, что дает
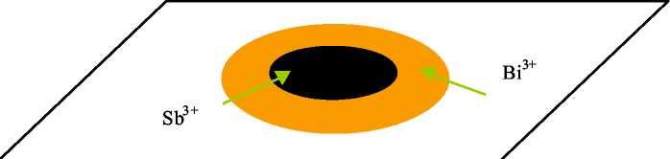
распределение ионов в виде концентрических зон (рис. 3.1).
В зависимости от
произведения растворимости осадка
или в зависимости
константы
устойчивости комплексных соединений:
чем больше их значения, тем ближе к центру
или в центре определенная зона. Капельный метод разработал советский ученый
химик Н.А. Тананаев.
Рис. 3.1. Схема образования окрашенных зон при действии на исследуемый раствор с
катионами Sb
+3
, Bi
+3
реагента (NH
4
)
2
S.
Реакции методом растирания.
Небольшое количество твердого вещества
растирают на фарфоровой пластинке или в ступке с примерно равным количеством

