Упрощенная HTML-версия
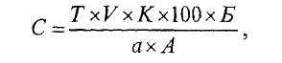
разведенной серной кислоты в мерной колбе вместимостью 1 л доводят объем
раствора водой до метки.
2.
Бюретку заполнить раствором ЭДТА, установить уровень раствора на
“0” отметке.
3.
Мерной пипеткой перенести аликвоты стандартного раствора ZnSO
4
точно по 10.00 мл в каждую коническую колбу для титрования.
4.
В каждую колбу для титрования добавить 30-40 мл дистиллированной
воды и раствор аммиака (2%-й) для нейтрализации серной кислоты до
рН≥6 по универсальной индикаторной бумаге.
5.
В колбы для титрования отмерить мерным цилиндром по 10 мл
аммиачного буферного раствора и раствор индикатора (или на кончике
шпателя – сухой индикатор) до отчетливой розовой окраски.
6.
Оттитровать каждую аликвоту раствором ЭДТА из бюретки (начиная
от “0” отметки) до перехода розовой окраски в голубую; записать
объем израсходованного титранта.
Обработка результатов:
Рассчитать концентрацию стандартного раствора сульфата цинка:
C
(ZnSO
4
) =
)
(ZnSO
(Zn)
(Zn)
4
V M
m
Рассчитать концентрацию стандартизованного раствора ЭДТА:
C
(ЭДТА) =
C
(ZnSO
4
)
V
(ZnSO
4
)
аликв
/
V
(ЭДТА)
средн
Примеры применения комплексонометричесго метода
в количественном анализе веществ
Прямое титрование: СаCl
2
6Н
2
О – определяемое вещество, титрант - 0,05 М
раствор ЭДТА
Методика определения: точную навеску (а) кальция хлорида растворяют в мерной
колбе вместимостью 100мл. Берут 25 мл этого раствора мерной пипеткой и переносят в
колбу для титрования, добавляют 5 мл аммиачного буферного раствора и 0,1г индикатора
кислотного хромового темно-синего и титруют раствором ЭДТА из бюретки до сине-
фиолетового окрашивания.
Расчет процентного содержания вещества в процентах проводят по формуле
прямого титрования:
где
c
— содержание определяемого вещества в процентах (массо-объемных или
массовых),
V
— объем титрованного раствора,
Т
—титр по определяемому веществу,
К
—поправочный коэффициент титрованного раствора,
а
— навеска (в г или мл) анализируемого средства.
Б
— объем мерной колбы (в мл),
А
— объем раствора, взятого на анализ (в мл).
Обратное титрование применяют, когда невозможно подобрать индикатор или
реакция комплексообразования протекает медленно. Сущность метода заключается в
добавлении к раствору определяемого вещества (а – точная навеска) избытка
титрованного раствора ЭДТА (V
1
), затем избыток титрованного раствора ЭДТА

